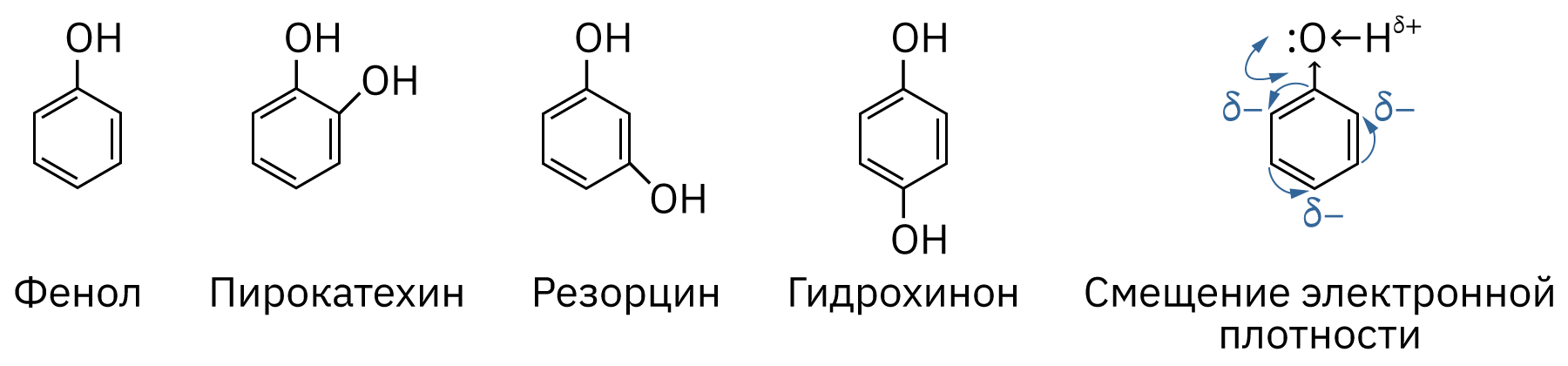
- Фенолы – производные ароматических углеводородов, в которых один или несколько атомов водорода замещены гидроксильной группой.
- Неподелённая пара электронов атома кислорода образует с π-электронным облаком бензольного кольца общую систему электронов. В результате смещения электронной плотности фенол проявляет слабые кислотные свойства, электронная плотность в бензольном кольце возрастает в орто- и пара- положениях, что облегчает взаимодействие с электрофилами.
Фенол – твёрдые бесцветные кристаллы с характерным запахом, плохо растворим в воде, ядовит, вызывает ожоги кожи.
- Фенол реагирует с щелочными металлами и щелочами:
2С6Н5–ОН + 2Na → 2С6Н5–ОNa + Н2↑; С6Н5–ОН + NaOH → С6Н5–ОNa + H2O.
- Качественная реакция:
6С6Н5ОН + FeCl3 → H3[Fe(C6H5O)6] + 3HCl – фиолетовый цвет.
- Бромирование, нитрование идёт легко в орто- и пара- положения.
- При каталитическом гидрировании образуется циклогексанол С6Н11ОН.
- В результате поликонденсации фенола с формальдегидом образуется фенолформальдегидная смола.